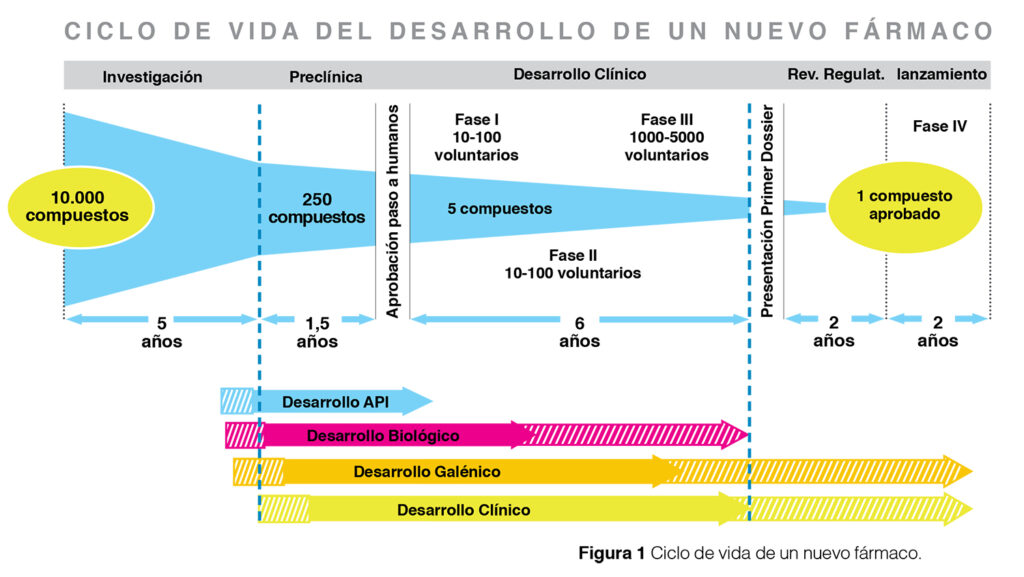
El desarrollo de medicamentos es un proceso complejo y riguroso que implica varias etapas, desde la investigación inicial hasta la comercialización y distribución. En este artículo, exploraremos cada una de estas etapas y cómo se garantiza la seguridad y eficacia de los medicamentos.
Investigación en medicamentos
La investigación en medicamentos es el primer paso en el desarrollo de nuevos fármacos. Los científicos investigan compuestos químicos y sustancias naturales en busca de posibles propiedades terapéuticas. Esta etapa incluye estudios de laboratorio y pruebas en modelos animales para determinar la seguridad y eficacia preliminar de los compuestos.
Desarrollo de medicamentos
Una vez identificados los compuestos prometedores, comienza el desarrollo de medicamentos. En esta etapa, se realizan estudios clínicos en humanos para evaluar la seguridad, dosis adecuada y eficacia de los medicamentos. También se lleva a cabo el diseño y fabricación de la forma farmacéutica final del medicamento, como pastillas o inyecciones.
Ensayos clínicos
Los ensayos clínicos son estudios realizados en voluntarios humanos para evaluar la seguridad y eficacia de un medicamento en desarrollo. Estos ensayos se dividen en varias fases, desde la fase I (donde se evalúa la seguridad y dosis) hasta la fase III (donde se evalúa la eficacia en un grupo más grande de pacientes). Los resultados de los ensayos clínicos son cruciales para obtener la aprobación regulatoria.
Regulaciones y aprobación
Antes de que un medicamento pueda ser comercializado, debe obtener la aprobación de las autoridades regulatorias. Estas autoridades, como la Administración de Alimentos y Medicamentos (FDA) en Estados Unidos, revisan los datos de seguridad y eficacia de los ensayos clínicos para garantizar que el medicamento sea seguro y efectivo para su uso en la población objetivo. Este proceso puede llevar varios años y requiere cumplir con estándares estrictos.
Comercialización y distribución
Una vez que un medicamento ha sido aprobado, comienza la etapa de comercialización y distribución. Las compañías farmacéuticas diseñan estrategias de marketing y establecen acuerdos con distribuidores y farmacias para asegurar la disponibilidad del medicamento en el mercado. También se llevan a cabo programas de educación médica para informar a los profesionales de la salud sobre el uso adecuado del medicamento.
Conclusión
El desarrollo de medicamentos es un proceso largo y complejo que requiere una investigación exhaustiva, ensayos clínicos rigurosos y la aprobación regulatoria. Aunque puede llevar años desarrollar un nuevo medicamento, este proceso es esencial para garantizar la seguridad y eficacia de los medicamentos que utilizamos.
Preguntas frecuentes
1. ¿Cuánto tiempo lleva desarrollar un nuevo medicamento?
El desarrollo de un nuevo medicamento puede llevar entre 10 y 15 años, desde la etapa de investigación hasta la comercialización.
2. ¿Cómo se garantiza la seguridad y eficacia de los medicamentos?
La seguridad y eficacia de los medicamentos se garantiza a través de ensayos clínicos rigurosos y la aprobación de las autoridades regulatorias, como la FDA.
3. ¿Qué papel juegan los ensayos clínicos en el desarrollo de medicamentos?
Los ensayos clínicos son fundamentales en el desarrollo de medicamentos, ya que proporcionan datos sobre la seguridad y eficacia del medicamento en poblaciones humanas.
4. ¿Cuáles son los principales desafíos en la comercialización de medicamentos?
Algunos de los principales desafíos en la comercialización de medicamentos incluyen la competencia en el mercado, la educación médica y la accesibilidad para los pacientes.